双靶点ADC药物迈向III期;康宁杰瑞JSKN016首例给药完成;三阴性乳腺癌治疗迎来潜在突破
免责声明:本文不构成投资建议,仅供医疗健康知识分享,以公司官方公告为准。内容非诊疗推荐,转载需授权。
在肿瘤药物研发领域,创新ADC药物的进展总是备受关注。康宁杰瑞制药最近公布,其自主开发的双特异性抗体偶联药物JSKN016,已在针对三阴性乳腺癌的III期临床试验中成功完成首例患者给药。这一事件标志着该药物从早期探索正式转向大规模验证阶段,也反映出公司在复杂ADC分子设计上的积累开始转化为临床价值。三阴性乳腺癌因缺乏激素受体和HER2表达,传统靶向治疗效果有限,患者亟需新型机制药物介入,而双靶点策略正为此提供可能路径。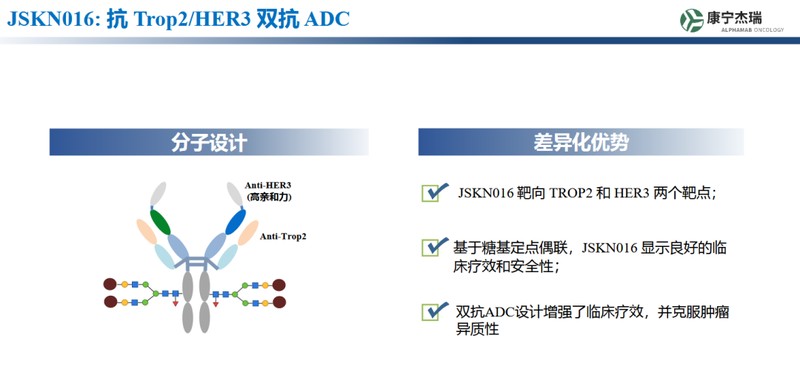

JSKN016-301试验采用多中心、随机、对照的开放设计,覆盖中国约六十家研究机构。入组对象主要为经多线治疗失败的晚期或转移性TNBC患者,试验将JSKN016与当前常用方案进行头对头比较,以评估其在疗效、耐受性和生活质量改善方面的综合表现。该药物的双靶向特性针对TROP2和HER3两种在肿瘤中高表达的受体,通过协同阻断信号通路并递送强效毒素,有望实现比单靶点药物更强的肿瘤杀伤力,同时降低脱靶风险。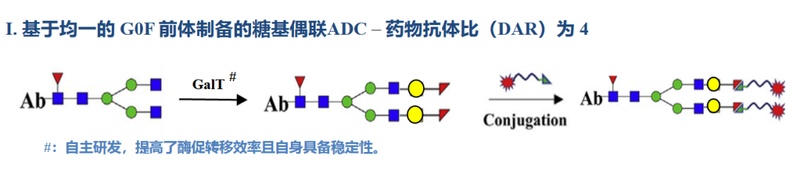
从技术层面看,JSKN016体现了康宁杰瑞在抗体工程和偶联技术上的独特优势。公司采用单域抗体构建双特异性分子,并运用自有糖基定点偶联平台,确保药物结构均一、DAR稳定在4。这一设计有效提升了ADC的药代动力学表现和体内安全性。在亲和力调控上,HER3端使用高亲和纳米抗体,而TROP2端亲和力适中,避免了常见于口腔等正常组织的毒性反应,提升了临床可及性。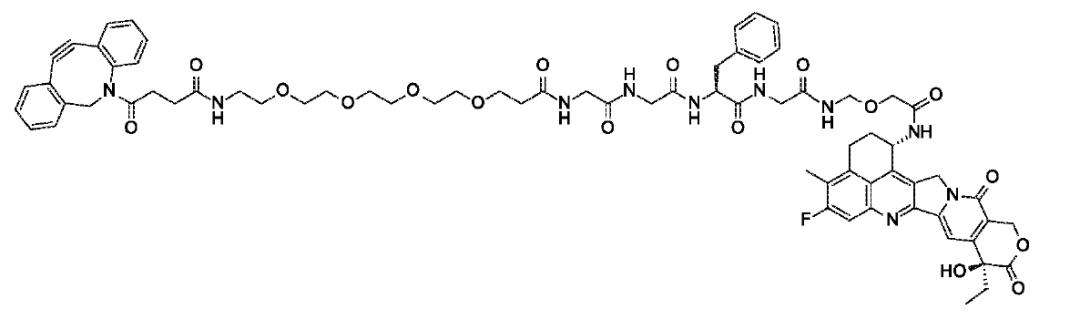

载荷部分选用拓扑异构酶I抑制剂,并辅以PEG修饰改善溶解度和分布特性。药物进入肿瘤细胞后,高效内吞并在溶酶体中释放载荷,精准干扰肿瘤DNA过程,导致细胞周期阻滞和凋亡。多项早期研究已证实JSKN016在晚期实体瘤患者中具有较好的抗瘤活性和耐受性,尤其在多线失败的TNBC亚群中观察到积极信号。这些数据为推动III期研究奠定了基础,也展示了双抗ADC在克服耐药机制方面的潜力。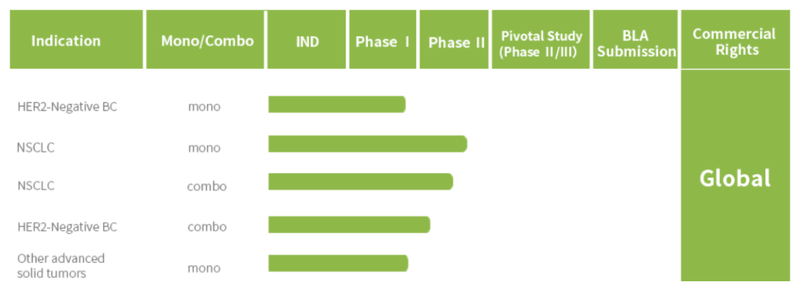

除了TNBC适应症,JSKN016还在肺癌、胃癌等其他实体瘤开展多项II期试验,探索单药及联合用药模式。随着临床管线逐步丰富,该药物有望构建更广泛的治疗网络。康宁杰瑞的这一进展,不仅强化了其在ADC领域的竞争力,也为中国生物制药产业在全球肿瘤创新竞争中增添了砝码。期待后续试验数据逐步揭晓,为患者带来更多获益机会。

总体上,双靶点ADC的临床推进体现了精准医学从概念到实践的深化。JSKN016的开发历程展示了技术创新与患者需求的紧密结合,未来若验证成功,将进一步推动三阴性乳腺癌治疗范式的演进。研发团队的持续努力值得肯定,这一里程碑也激励更多创新药物加速走向临床应用。



